Para poder comprender las leyes
que rigen los cambios en los gases cuando existen cambios en la temperatura o presión,
necesitamos saber más acerca de esta última. La presión se define como fuerza
la fuerza por unidad de área. Por ejemplo usted puede llenar las llantas su
auto a 32 lb/pilg2 (libras (fuerza) por pulgada cuadrada).
Manejaremos tres variables el
volumen la temperatura y la presión.
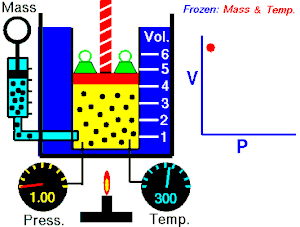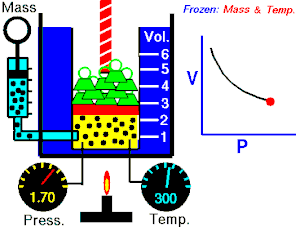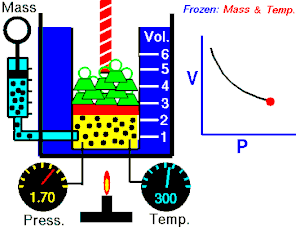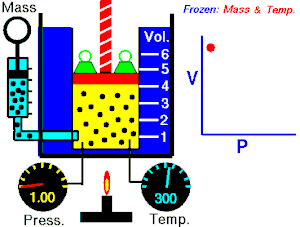
El impacto de las moléculas sobre
las paredes del recipiente que contiene el gas es lo que origina la presión
(con la cámara de aire). A mayor frecuencia de las colisiones, mayor presión
del gas. A meno frecuencia de las colisiones menor presión del gas.
Todos los gases ejercen al menos
una pequeña presión. Aun los gases de la atmósfera (principalmente nitrógeno,
el oxígeno y una pequeña cantidad de argón, además de cantidades pequeñas de
otros gases) ejercen sobre “su recipiente”.
Presión: fuerza por unidad de
área, ya sea que se exprese como libras por pulgada cuadrada (psi), centímetros
de mercurio (cm Hg), milímetros de mercurio (mm Hg), torr, pulgadas de mercurio
(pulg. Hg), atmosferas (atm), pascales (Pa) o milibares (mbar).
Barométrica.
Se define como la fuerza (F)
ejercida sobre determinada superficie (A). En el caso de la atmosfera; esta
capa gaseosa ejerce presión sobre cualquier punto de la superficie terrestre.
La presión atmosférica se mide
con barómetro de mercurio, que fue diseñado en 1643 por el matemático y físico
italiano evangelista Torricelli (1608-1647). Su barómetro estaba formado por un
largo tubo de vidrio cerrado en un extremo, lleno de mercurio, he invertido por
el extremo abierto sobre un recipiente de mercurio. A nivel del mar el tubo se
llegaba a una altura de 76.0 cm.
 |
| Obtenida de: http://hyperphysics. |
En repetidas ocasiones los
experimentos con tubos de diferentes diámetros revelaron un fenómeno
importante: sin importar el diámetro del tubo, el nivel de mercurio llegaba a
76 cm. Para comprender esto utilizamos un tubo cerrado con un diámetro de 1.13
cm. El volumen del mercurio dentro del tubo a nivel del mar seria 76.0 cm x
1.00cm2 = 76 cm23.
Manométrica.
Se usan utilizan diversos
dispositivos para medir las presiones de gases encerrados en un recipiente. Los
sencillos medidores que se emplean para medir la presión del aire en las
llantas de los automóviles indican presiones mayores y menores a la presión
atmosférica.
En los laboratorios un
dispositivo sencillo llamado manómetro, cuyo principio de operación es similar
al del barómetro.
En la figura a) se ilustra un
manómetro de tubo cerrado, dispositivo que para medir presiones inferiores a la
presión atmosférica.
 |
| Obtenida de: https://alejandragongora.files.wordpress.com/2014/08/eb57265122.gif |